 1,*
1,*Artículos de Investigación
Resultados preliminares del ambiente acústico enriquecido como terapia sonora personalizada del acúfeno
EAE como terapia sonora del acúfeno
1Instituto de Tecnologías Físicas y de la Información (ITEFI), Consejo Superior de Investigaciones Científicas (CSIC), Serrano 144, 28006 Madrid, España
 OPEN ACCESS
OPEN ACCESS
PEER REVIEWED
INFORME DE INVESTIGACIÓN
Resumen
El objetivo de este artículo es describir los fundamentos de una terapia sonora, el ambiente acústico enriquecido (EAE), para la estimulación selectiva de pacientes con acúfenos. El estímulo sonoro consiste en una secuencia de tonos, que pueden ser de tres tipos (pip, burst o gamma), de frecuencia aleatoria dentro de la banda de frecuencias audibles, cada uno de ellos con una amplitud directamente proporcional a la pérdida de audición del sujeto a esa frecuencia. Las secuencias de tonos pip y tonos burst ya han demostrado su eficacia en la restauración del mapa tonotópico de animales expuestos previamente a un ruido traumatizante y en el restablecimiento de la hipersensibilidad de un grupo de pacientes con hiperacusia, respectivamente. Las secuencias de tonos gamma, cuyos fundamentos se describen en este artículo, constituyen una propuesta original. La sucesión de tonos resultante estimula secuencialmente el sistema auditivo del sujeto compensando su pérdida de audición, que es una de las causas que disparan el acúfeno.
Palabras clave
Acúfeno, terapia sonora, ambiente acústico enriquecido
Implicaciones clínicas
El artículo describe una terapia sonora personalizada para el acúfeno que puede aplicarse en la propia clínica del especialista. Para ello, se recibe al paciente en la clínica, se le miden las audiometrías de ambos oídos y se diseña el estímulo EAE estéreo, el cual se entrega al paciente en formato mp3 para que lo escuche una hora al día durante cuatro meses. Para el seguimiento, se requiere al paciente un THI mensual que puede rellenar en casa y enviar por correo electrónico.
Recibido: 15.07.2021 Revisado: 18.08.2021 Aceptado: 24.08.2021 Publicado: 13.10.2021
Editado por:
Helia Relaño-Iborra
Universidad Técnica de Dinamarca
Revisado por:
Patricia Vázquez-González
Fundación Vinjoy, España
Juan Manuel Espinosa-Sanchez
Universidad de Granada, España
María Teresa Heitzmann Hernández
Clínica Universidad de Navarra, España
1. Introducción
Algunas personas han percibido ocasionalmente un zumbido en los oídos que no viene del exterior del sistema auditivo y que puede estar asociado a alguna causa reversible, como la exposición a un ruido muy alto (concierto de música, fuegos artificiales) o una perturbación transitoria del oído (Eggermont, 2012). Sin embargo, en un porcentaje de la población, este ruido interior, una vez que se ha originado, no remite. La percepción de un sonido en ausencia de una fuente acústica externa se denomina acúfeno (tinnitus) y es más prevalente en la población mayor (12% en los mayores de 60 años) que en la más joven (5% entre 20 y 30 años; Baguley et al., 2013). En el 1%-2% de la población, la gravedad del acúfeno es tal que afecta a la calidad de vida, produciendo molestia, problemas con el sueño, estrés, ansiedad o depresión. En los EE. UU., entre 25 y 52 millones de personas padecen de acúfenos (Jastreboff y Jastreboff, 2000), mientras que en Europa se estima que unos 5 millones experimentan un zumbido moderado o grave (Vio and Holmes, 2015). En España, el 17% de los pacientes de una consulta de ORL manifestaban este tipo de ruidos (Herráiz y Hernández Calvín, 2002), mientras que, en el 1% de pacientes, el acúfeno es altamente invalidante (López González, 2010).
Así pues, el acúfeno crónico (el que se percibe de una manera prolongada o continua durante más de tres meses) puede producir una reducción considerable de la calidad de vida de quien lo padece. Se ha demostrado que los daños producidos en el sistema auditivo periférico de un grupo de animales de laboratorio por la exposición a un ruido traumatizante daban lugar a cambios funcionales en su mapa tonotópico cortical (Noreña y Eggermont, 2005). La capacidad de cambio del sistema auditivo cortical y subcortical se denomina plasticidad auditiva. La sobreexposición a ruido, el envejecimiento, la infección del oído, la ototoxicidad y la enfermedad de Ménière, entre otros, producen pérdidas de audición (en inglés hearing loss; HL) periféricas que dan lugar a una desaferenciación del sistema auditivo central, lo que puede suponer un posible desencadenante de acúfenos.
La HL es reconocida como un factor de riesgo para el acúfeno (Tan et al., 2013). Sin embargo, hay muchos individuos con HL que no sufren de acúfenos. En pacientes con HL neurosensorial la prevalencia del acúfeno es mayor, y su timbre es más alto (>3 kHz), que en aquellos con HL conductiva, en los cuales el timbre es más bajo (< 1 kHz; Cuesta y Cobo, 2018). Parece entonces que la relación del acúfeno con la HL es más compleja y que pueden existir otros factores, tales como alteraciones en las sinapsis entre las células ciliadas y las fibras del nervio auditivo que pueden contribuir a la aparición del acúfeno (Paul et al., 2017).
Los substratos neurales del acúfeno sugieren varias aproximaciones para modificar el procesamiento neural y cambiar sus propiedades, obteniendo de este modo algún alivio. Aunque actualmente no existe ningún fármaco específico para la curación del acúfeno, se pueden usar aproximaciones neurofisiológicas o psicológicas para reducir sus efectos. Los tratamientos con base neurofisiológica incluyen métodos de sustitución para compensar la actividad perdida en la salida de la cóclea, vía ambientes acústicos especialmente diseñados, o amplificando el ambiente sonoro en los rangos de frecuencias perdidas mediante audífonos o algún otro dispositivo de generación de sonido. Las aproximaciones psicológicas están basadas en modelos neurofisiológicos del acúfeno o derivadas de paradigmas de tratamiento de personas con depresión. Usualmente se aplica conjuntamente con alguna terapia sonora (Jastreboff, 2015).
Se puede aprovechar la plasticidad para reducir la percepción del acúfeno estimulando adecuadamente la vía auditiva (Schaette y Kempter, 2006). Esto ha dado lugar a diferentes terapias sonoras, cuyo objetivo principal es producir habituación (Jastreboff, 1990) o inhibición residual (Henry, 2016). La habituación se produce al eliminar las connotaciones que inciden negativamente sobre la calidad de vida, actuando más sobre los sistemas límbico y autónomo, combinando el consejo terapéutico (habituación a la reacción) y el uso de terapia sonora (habituación a la percepción). Tiene que pasarse por estas dos etapas para conseguir ignorar el acúfeno (habituación). Enmascarando el acúfeno se puede conseguir que desaparezca su percepción. Una vez que cesa el estímulo se tarda un tiempo en volver a percibirlo, lo que se conoce como inhibición residual, que puede durar un tiempo variable (desde unos segundos hasta horas). La relación entre los parámetros del estímulo sonoro, tales como espectro, intensidad y duración y su efecto en el acúfeno, no se conoce muy bien (Henry, 2016), lo que ha dado lugar a proponer un gran número de terapias sonoras (Pienkowski, 2019).
El objetivo principal de este artículo es exponer las bases de una terapia sonora basada en las curvas de HL del paciente, especialmente apropiada para el acúfeno. Esta terapia sonora, denominada ambiente acústico enriquecido (EAE, por sus siglas en inglés), consiste en una secuencia de tonos de frecuencia aleatoria dentro de la banda de audición (la banda de frecuencias en la que se miden las HL) y una amplitud directamente proporcional al valor de la pérdida auditiva a esa frecuencia.
2. Materiales y Métodos
Noreña y Eggermont (2005) ya demostraron que un grupo de animales a los que previamente se los había expuesto a un ruido traumatizante que alteraba su mapa tonotópico cortical, cuando se introducían en un ambiente acústico enriquecido consistente en una secuencia aleatoria de tonos pip, recuperaban su mapa tonotópico normal. Noreña y Chery-Croze (2007), por otra parte, usaron una terapia sonora similar para revertir la hipersensibilidad padecida por un grupo de sujetos con hiperacusia. En este caso, el estímulo consistía en una secuencia de tonos burst de frecuencia aleatoria y amplitud proporcional a la pérdida de audición. En realidad, esta secuencia de tonos burst era una variante de la secuencia de tonos pip usada por Noreña y Eggermont en su modelo animal. A continuación se analizan más detalladamente las propiedades de los tonos pip y burst, y se motiva la introducción de una nueva secuencia, los tonos gamma.
2.1. Secuencias de tonos pip
Los tonos pip tienen la forma (Noreña y Eggermont, 2005)
donde α y γ son dos constantes que determinan la forma de onda del tono, y por tanto su espectro. Pues bien, una secuencia de tonos pip (STP) tiene la forma
donde fm es la frecuencia del tono pip elegida aleatoriamente dentro de la banda de interés, τm es el retardo de cada uno de ellos, o interlatencia entre los tonos, y Am es la amplitud de cada tono, dada por
siendo HL(fm) el valor de la pérdida auditiva a la frecuencia fm. Así pues, cada uno de los tonos pip está determinado por los parámetros (α,γ) y por la tasa de disparos (τ, número de tonos por segundo). En la mayor parte de los trabajos publicados se usa γ = 3. Para la tasa de pulsos, se suele usar una rápida (20 por segundo) y una lenta (1 por segundo).
2.2. Secuencias de tonos burst
Los tonos burst tienen por ecuación
donde w(t) es una ventana temporal (rectangular, Hanning, Hamming, etc.). Por tanto, una secuencia de tonos burst sería
donde, fm, τm y Am tienen el mismo significado que en las Ecs. (1-3). Noreña y Chery-Croze (2007) usaban una ventana, w(t), rectangular con rampas lineales de 5 ms de subida y bajada.
2.3. Secuencias de tonos gamma
Tanto los tonos pip como los burst estimulan selectivamente la vía auditiva. Sin embargo, el espectro de los tonos pip, determinado por el par de parámetros (α, γ), es más parecido a la curva de respuesta en frecuencias de diferentes partes de la vía auditiva (la membrana basilar, por ejemplo). Por otra parte, dicha curva de respuesta en frecuencia depende de la especie. Por tanto, una terapia EAE óptima para el acúfeno sería una basada en secuencias de tonos pip con el par de parámetros (α, γ)apropiados para el sistema auditivo humano. Los filtros gamma son precisamente eso tonos pip, con las variables (α, γ)apropiadas para el sistema auditivo humano. Específicamente, la ecuación para un tono gamma es
Cuando se transforma el tono gamma al dominio de la frecuencia se obtiene un filtro gamma de orden n, ancho de banda b, frecuencia central f0 y fase ϕ. Patterson (1994) demostró que un filtro auditivo humano se obtiene con un filtro gamma de orden n = 4 y ancho de banda rectangular equivalente (ERB), también denominado «banda crítica», dado por
Para simular el movimiento de la membrana basilar se suele usar un banco de filtros gamma distribuidos a lo largo del eje de frecuencias. Finalmente, se obtiene la siguiente ecuación para la secuencia de tonos gamma
donde fm, τm y Am ya han sido definidos en la sección 2.1, bm es el ancho de banda equivalente a la frecuencia fm obtenido utilizando la Ec. (7), y
2.4. Implementación del EAE como terapia sonora del acúfeno
Así pues, un EAE apropiado para la terapia de los acúfenos sería
donde fm, τm y Am son la frecuencia, retardo y amplitud de cada tono, y
es la envolvente de cada pulso. La figura 1 muestra los espectros de un tono pip, un tono burst y un tono gamma a la misma frecuencia (f0 = 500 Hz). Para el tono burst se ha usado una ventana de Blackman-Harris. Para el tono pip se usa el par de parámetros (α,γ) = (3,225). Los tres tonos muestran una cierta asimetría en escala logarítmica. No obstante, el tono gamma tiene un espectro ligeramente más ancho y con unas ramas izquierda y derecha más limpias.
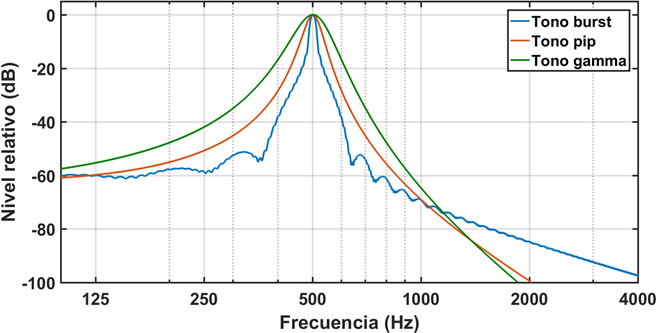
Figura 1: Espectros de un tono burst, un tono pip y un tono gamma, a la frecuencia de 500 Hz. Para el tono burst se usa una ventana del tipo Blackman-Harris. Para el tono pip se usa un par de parámetros (α, γ) = (3,225). El tono gamma viene completamente determinado por la frecuencia central de 500 Hz.
La figura 2 muestra los espectros de una secuencia de tonos gamma a diferentes frecuencias. En este caso se ha calculado una secuencia de 10 segundos, a una tasa de 4 pulsos por segundo. La secuencia contiene, por tanto, 40 tonos gamma. Como se puede comprobar, la amplitud de cada tono es proporcional al valor de la pérdida de audición a cada frecuencia. Un paciente de acúfenos con la HL de la figura 2, expuesto a una secuencia tal, percibiría todos los tonos al mismo nivel (sensación ecualizada de amplitud). Asumiendo que el acúfeno se desencadena esencialmente por el intento del sistema auditivo neural de compensar la privación periférica producida por la HL, el entrenamiento auditivo con este tipo de estímulo trabajaría en el sentido contrario, lo que ayudaría a la reducción progresiva de la percepción del acúfeno, y por consiguiente, a su habituación.
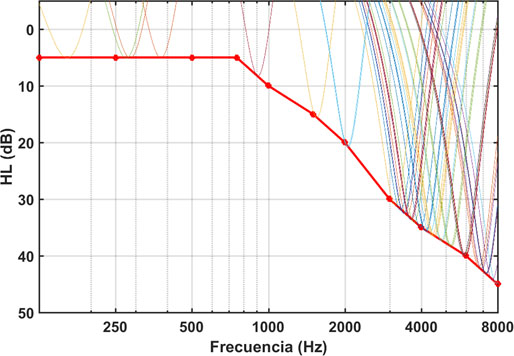
Figura 2: Espectros de una secuencia de tonos gamma superpuestos a la curva de HL correspondiente.
Cobo (2014) ha puesto a punto una interfaz gráfica de usuario (GUI), figura 3, para el diseño de una terapia EAE basada en secuencias de tonos burst, pip y gamma. Partiendo de las curvas de HL de los pacientes en cada oído, la GUI permite generar la EAE como una secuencia diótica o dicótica de tonos, reproducirla a través de la tarjeta de sonido del ordenador o guardarla como un archivo de audio para que el paciente la pueda escuchar a través de un equipo de sonido, según las indicaciones del especialista. La GUI incluye también una sección de propiedades de la señal en la cual se pueden introducir la frecuencia de muestreo, en Hz, la longitud de la señal, en s, y la tasa de pulsos por segundo. En otra sección se dibujan las curvas de HL de cada oído del paciente, lo que permite un mejor control visual de su capacidad auditiva.
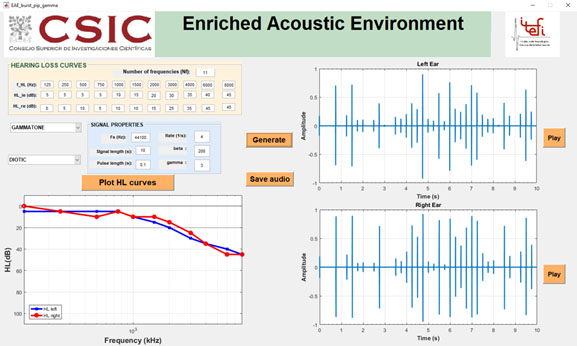
Figura 3: GUI para el diseño de un EAE para la terapia sonora del acúfeno basado en una secuencia de tonos.
Resultados
En el año 2018 se inició un estudio clínico, con la aprobación del Subcomité de Bioética del CSIC, para probar la terapia EAE en pacientes de acúfenos de etiología variada. Todos los participantes de este estudio firmaron un consentimiento informado. Hasta ahora se han reclutado 140 pacientes de los cuales fueron excluidos 20 por diferentes causas. A los 120 restantes se les sometió a un tratamiento combinado de consejo terapéutico y terapia sonora. El consejo terapéutico, que se aplicó en una sesión única de unos 60 minutos al inicio del tratamiento, consistió en una presentación en la que se les explicaban los mecanismos, epidemiología y etiología del acúfeno, así como los fundamentos de la terapia sonora EAE. La terapia sonora personalizada consistió en una EAE basada en una secuencia binaural de tonos burst, pip o gamma. Los pacientes elegían el más confortable de los tres tipos de tonos. La prescripción fue oír este estímulo una hora al día durante cuatro meses. Abandonaron el tratamiento 34 pacientes antes de su finalización y otros 11 no lo han acabado todavía. Se les realizó un control mensual a través de la versión española del cuestionario Tinnitus Handicap Inventory (THI) (Herráiz et al., 2001). El THI es un cuestionario de 25 preguntas diseñado para medir la angustia, el hándicap y las consecuencias sicosociales del acúfeno (Newman et al., 1998). De acuerdo con la escala de gravedad del acúfeno propuesta por McCombe et al. (2001), 18 ≤ THI ≤ 36 correspondería a un acúfeno leve, 38 ≤ THI ≤ 56 a un acúfeno moderado, 58 ≤ THI ≤ 76 a un acúfeno severo, THI ≥ 78 a un acúfeno catastrófico.
Los resultados en los 75 pacientes que han completado el tratamiento son muy prometedores y están bajo revisión en otra revista científica. A modo de ilustración se presentan aquí los resultados preliminares en tres pacientes sometidos a un EAE de tonos pip y gamma.
El paciente n.º 1 es un varón de 44 años que fue reclutado para nuestro estudio en enero de 2018. Su acúfeno, localizado en el oído derecho, surgió en noviembre de 2015, coincidiendo con una época de estrés alto. Previamente, había sufrido una estapedectomía del oído derecho en el año 2012. Sus audiometrías, figura 4A, mostraban una audición normal en el oído izquierdo y unas pérdidas moderadas en frecuencias altas en el oído derecho. Eligió ser tratado con una secuencia de tonos pip, con parámetros (α, γ) = (3,200). Después de los cuatro meses de tratamiento con este EAE, su THI se redujo desde un valor inicial de 36 hasta un valor final de 18, figura 5.
El paciente n. 2 es un varón de 60 años que ingresó en nuestro estudio en julio de 2019. Tenía un acúfeno en el oído izquierdo desde hacía tres años que surgió después de un episodio de vértigo por enfermedad de Ménière. Sus audiometrías, figura 4B, muestran una audición normal en el oído derecho, en frecuencias bajas y medias, y una pérdida ligera a moderada a frecuencias altas. En el oído izquierdo, sin embargo, presenta pérdidas de moderadas, a frecuencias bajas, a profundas, a frecuencias altas. Después de seguir un tratamiento EAE con una secuencia de tonos gamma, su THI experimentó una bajada de 34 puntos, figura 5, desde un valor inicial de 68 hasta un valor final de 34.
El paciente n. º3 es una mujer de 42 años que solicitó ingresar en nuestro estudio en marzo de 2021. Padecía un acúfeno en el oído izquierdo desde hacía un año y medio. En diciembre de 2019 fue diagnosticada de una neuritis vestibular, que le causó vértigos y acúfeno. Sus audiometrías, figura 4C, muestran una audición normal en el oído derecho con un ligero escotoma en 4 kHz y pérdidas ligeras a frecuencias altas en el oído izquierdo. La gravedad de su acúfeno se incrementó en noviembre de 2020, coincidiendo con su contagio del COVID-19. Se sometió a una terapia EAE basada en una secuencia de tonos gamma entre Marzo y Julio de 2021. Su THI experimentó una bajada de 40 puntos, desde un valor inicial de 46 hasta un valor final de 6 (Figura 5).
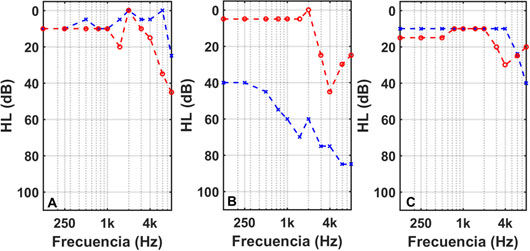
Figura 4: Curvas de HL de los oídos izquierdo (línea azul) y derecho (línea roja) de los tres pacientes sometidos a la terapia EAE del acúfeno.
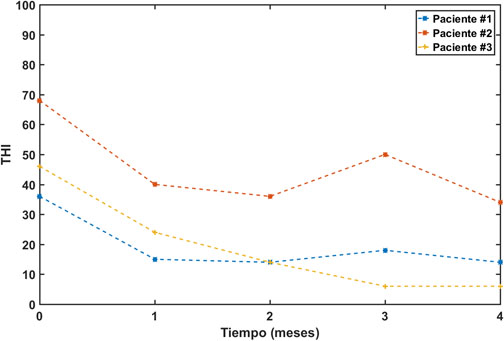
Figura 5: Evolución del THI de los tres pacientes sometidos a la terapia EAE del acúfeno.
Discusión
La terapia EAE, como la de Reentrenamiento del Acúfeno (TRT), se aplica en combinación con el consejo terapéutico (Jastreboff, 2015). La diferencia principal entre ambos tratamientos radica en el tipo de estímulo que se usa en la terapia sonora. El estímulo usual en la TRT es un ruido de banda ancha, aunque también se han usado otros estímulos, tales como sonidos coloreados (Henry et al., 2004) o filtrados en una banda más estrecha (Kim et al., 2014), y música espectralmente alterada (Li et al., 2016). Mientras que el ruido de banda ancha es válido para cualquier tipo de paciente, el estímulo EAE se basa en las pérdidas de audición, y por tanto, es personalizado para cada sujeto. Aunque cualquier tipo de sonido es mejor que el silencio como terapia sonora del acúfeno, con tal de que no produzca daños o moleste (Jastreboff y Jastreboff, 2000), el estímulo EAE incorpora la compensación por la pérdida auditiva, por lo que es más selectivo que el ruido de banda ancha.
La terapia EAE se implementa mediante una secuencia de tonos pip, burst o gamma, a elegir por el paciente. Las secuencias de tonos pip y gamma ya fueron usadas por otros autores (Noreña y Eggermont, 2005; Noreña y Chery-Croze, 2007). Los tonos pip, que fueron usados esencialmente en modelos animales, son más selectivos que los tonos gamma y tienen una envolvente (y por tanto, un espectro) que depende de dos parámetros (α,γ). Estos parámetros toman unos valores que varían para cada especie animal ensayada. La aplicación directa de estos tonos pip para la terapia sonora del acúfeno requiere, por tanto, asignar el valor apropiado a estos parámetros para la especie humana. La aportación más novedosa de este trabajo es la incorporación de los tonos gamma, en los cuales la forma de onda (y el espectro) de cada uno de los tonos está determinada exclusivamente por la frecuencia del tono. Por tanto, mientras que los parámetros de los tonos pip están indefinidos, puesto que dependen de la especie ensayada, en los tonos gamma, están perfectamente definidos.
La duración del tratamiento EAE que estamos proponiendo (una hora al día, durante cuatro meses) es mucho más corta comparada con otras encontradas en la literatura. Henry et al. (2006), Bauer et al. (2017) y Oishi et al. (2013), por ejemplo, presentaron los resultados de estudios clínicos usando la TRT durante 18 o 24 meses. Sin embargo, usando un estímulo personalizado, como el EAE, se puede conseguir un efecto clínicamente relevante (reducción del THI mayor que 20 puntos) en un tiempo mucho más corto.
En este artículo se presentan resultados de reducción del THI para tres pacientes cuyo acúfeno se generó después de un episodio de estrés (paciente n.º 1), enfermedad de Ménière (paciente n. º2) y neuritis vestibular (paciente n.º 3). No obstante, al igual que la TRT, la terapia EAE se puede aplicar a pacientes de acúfenos de cualquier etiología (Jastreboff, 2015). Las únicas restricciones (criterios de exclusión) son operaciones quirúrgicas (menos de tres meses), episodios de vértigo recientes (menos de 15 días), o hidrocefalia. Además, se consideran criterios excluyentes la edad menor que 18 y mayor que 75 años, y la gravedad del acúfeno (THI < 20).
Los tonos de la secuencia EAE incluyen un factor de amplitud que es proporcional a la pérdida de audición del paciente en cada frecuencia. Así mismo, como el estímulo es estéreo, se incluye la diferente sensibilidad de cada oído. El resultado es un estímulo estéreo que produce una sensación ecualizada en ambos oídos en todas las frecuencias. Este estímulo ecualizado es apropiado para pacientes con pérdidas de ligeras a moderadas y que no padecen de tolerancia reducida al sonido (hiperacusia o misofonía). En pacientes con hiperacusia o misofonía, o con pérdidas de audición graves o profundas, hay que tener cuidado para no amplificar excesivamente los pulsos de la secuencia. En estos casos, la amplitud de los tonos se ajusta como un compromiso entre la compensación de la pérdida auditiva y el umbral de intolerancia al sonido.
Conclusiones
El ambiente acústico enriquecido consiste en una secuencia de tonos (pip, burst o gamma) de frecuencia aleatoria dentro de la banda de audición y amplitud proporcional a la pérdida de audición en esa frecuencia. El espectro de cada tono gamma en una frecuencia es un filtro gamma que estimula selectivamente el sistema auditivo en esa frecuencia. Por tanto, una secuencia de tonos gamma con amplitudes que compensan la pérdida de audición del paciente en cada frecuencia constituye el estímulo sonoro personalizado óptimo para la terapia sonora del acúfeno.
Referencias
Baguley, D., McFerran, D, Hall, D. (2013). Tinnitus. Lancet, 382, 1600-1607. http://dx.doi.org/10.1016/S0140-6736(13)60142-7.
Bauer, C.A., Berry, J.L., Brozowski, T.J. (2017). The effect of Tinnitus Retraining Therapy on chronic tinnitus: A controlled trial. Laryngoscope Investig. Otolaryngol., 2, 166-177. doi: 10.1002/lio2.76.
Cobo, P. (2014). Ambiente Acústicamente Enriquecido para la terapia sonora del acúfeno. IX Congreso Iberoamericano de Acústica, FIA 2014, Valdivia (Chile).
Cuesta, M., Cobo, P. (2018). Relating tinnitus features and audiometric characteristics in a cohort of 34 tinnitus subjects. Loquens, 5, e054. https://doi.org/10.3989/loquens.2018.054
Eggermont, J.J. (2012). The Neuroscience of Tinnitus. Oxford University Press, Oxford (UK).
Henry, J.A., Rheinsburg, B., Zaugg, T. (2004). Comparison of custom sounds for achieving tinnitus relief. J. Am. Acad. Audiol., 15, 585-598. doi: 10.3342/ceo.2014.7.2.87.
Henry, J.A., Schechter, M.A., Zaugg, T.L., Griest, S., Jastreboff, P.J., Vernon, J.A., Kaelin, C., Meikle, M.B., Lyons, K.S., Stewards, B.J. (2006). Outcomes of clinical trial: Tinnitus Masking versus Tinnitus Retraining Therapy. J. Am. Acad. Audiol., 17, 104-132. doi: 10.3766/jaaa.17.2.4.
Henry, J.A. (2016). Measurement of tinnitus. Otol. Neurotol., 37, e276-e275. doi: 10.1097/MAO.0000000000001070.
Herráiz, C., Hernández Calvín, F.J., Plaza, G., Tapia, M.C., De los Santos, G. (2001). Evaluación de la incapacidad en los pacientes con acufenos. Acta Otorrinolaringol. Esp., 52, 142-145. doi: 10.1016/S0001-6519(01)78247-7.
Herráiz, C., Hernández Calvín, F.J. (2002). Acúfenos: Actualización. Ars Médica (Madrid).
Jastreboff, P.J. (1990). Phantom auditory perception (tinnitus): mechanisms of generation and perception. Neurosci. Res., 8, 221-254. doi: 10.1016/0168-0102(90)90031-9.
Jastreboff, P.J, Jastreboff, M.M. (2000). Tinnitus Retraining Therapy (TRT) as a method for treatment of tinnitus and hyperacusis patients. J. Am. Acad. Audiol., 11, 162-177.
Jastreboff, P.J. (2015). 25 years of tinnitus retraining therapy. HNO, 63, 307-311. doi: 10.1007/s00106-014-2979-1.
Kim, B.J., Chung, S.W., Jung, J.Y., Suh, M.W. (2014). Effect of different sounds on the treatment outcome of tinnitus retraining therapy. Clin. Exp. Otorhinolaryngol., 7, 87-93. doi: 10.3342/ceo.2014.7.2.87.
Li, S.A., Bao, L., Chrostowski, M. (2016). Investigating the effects of a personalized, spectrally altered music-based sound therapy on treating tinnitus: A blinded, randomized controlled trial. Audiol. Neurootol., 21, 296-304. doi: 10.1159/000450745.
López González, M.A. (2010). Factores etiopatogénicos de acúfenos. En Acúfeno como Señal de Malestar (López González y Esteban Ortega, Eds.), Capítulo 3, 22-30, CC2010, Sevilla.
McCombe, A., Baguley, D., Coles, R., McKeyna, L., McKinney, C., Windle-Taylor, P. (2001). Guidelines for the grading of tinnitus severty: the results of a working group commisioned by the British Association of Otolaryngologists. Clin. Otolaryngol. Allied Sci., 26, 388-93. doi: 10.1046/j.1365-2273.2001.00490.x.
Newman, C.W., Sandridge, S.A., Jacobson, G.P. (1998). Psychometric adequacy of the Tinnitus Handicap Inventory (THI) for evaluating treatment outcome. J. Am. Acad. Audiol., 9, 153-60.
Noreña, A.J., Eggermont, J.J. (2005). Enriched acoustic environment alter noise trauma reduces hearing loss and prevents cortical map reorganization. J. Neurosci., 25, 699-705. doi:10.1523/JNEUROSCI.2226-04.2005.
Noreña, A.J., Chery-Croze, S. (2007). Enriched acoustic environment rescales auditory sensitivity. NeuroReport, 18, 1251-1255. doi: 10.1097/WNR.0b013e3282202c35.
Oishi, N., Shinden, S., Kanzaki, S., Saito, K., Inoue, Y., Ogawa, K. (2013). Effects of tinnitus retraining therapy involving monaural noise generators. Eur. Arch. Otorhinolaryngol., 270, 443-448. doi: 10.1007/s00405-012-1951-5.
Patterson, R.D. (1994). The sound of a sinusoid: Spectral models. J. Acoust. Soc. Am., 96, 1409-1418. https://doi.org/10.1121/1.410285.
Paul, B.T., Bruce, I.C., Roberts, L.E. (2017). Evidence that hidden hearing loss underlies amplitude modulation encoding deficits in individuals with and without tinnitus. Hear. Res., 344, 170-182. https://doi.org/10.1016/j.heares.2018.04.005.
Pienkowski, M. (2019). Rationale and efficacy of sound therapies for tinnitus and hyperacusis. Neurosci., 407, 120-34. https://doi.org/10.1016/j.neuroscience.2018.09.012.
Schaette, R., Kempter, R. (2006). Development of tinnitus-related neuronal hyperactivity through homeostatic plasticity after hearing loss: a computational model. Eur. J. Neurosci., 23, 3124-3138. doi: 10.1111/j.1460-9568.2006.04774.x.
Tan, C.M., Lecluyse, W., McFerran, D., Meddis, R. (2013). Tinnitus and patterns of hearing loss. JARO, 14, 275-282. doi: 10.1007/s10162-013-0371-6.
Vio, M.M., Holmes, R.H. (2015). Hearing loss and tinnitus: 250 million people and a US$10 billion potential market. Drug Discovery Today, 10, 1263-1265. doi: 10.1016/S1359-6446(05)03594-4.
Conflicto de interés
El autor declara no tener ningún conflicto de interés.
Fondos
Esta investigación no ha recibido fondos externos.
Agradecimientos
Se agradece la participación de los pacientes en este estudio.
Citar como:
Cobo, P. Resultados preliminares del ambiente acústico enriquecido como terapia sonora personalizada del acúfeno: EAE como terapia sonora del acúfeno. Auditio, 5(3).
Tipo de Licencia: Atribución 4.0 https://creativecommons.org/licenses/by/4.0/
Correspondencia:
*Pedro Cobo
ITEFI (CSIC), Serrano 144, 28006 Madrid, España
Teléfono: +34 91 5618806
email: pedro.cobo@csic.es
Oficina Editorial
Revision ortotipografica: Tomás Pérez Pazos
Traducción: Louis M. de Ladebauche
Producción: Publicaciones Académicas